がん免疫療法コラム


新たなCAR-T療法用の再生医療等製品の誕生
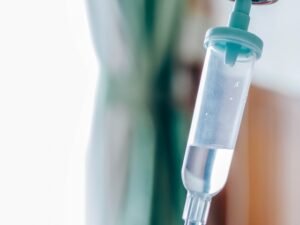
国内2番目のCAR-T療法用の再生医療等製品が誕生
「CAR-T 療法」という言葉に見覚えがある方は多いのではないでしょうか?
CAR-T とはキメラ抗原受容体導入T細胞 (Chimeric antigen receptor T cell)療法の略称で、 特定のがん細胞に対して十分な免疫応答を示すために患者さん自身の T 細胞を改変する治療法です。
日本では、2019年3月にノバルティス ファーマのキムリアがCAR-T療法用の再生医療等製品として初めて承認され、キムリア治療提供可能施設で治療を受けることができます。そして、2021年1月に国内2番目のCAR-T療法用の再生医療等製品として第一三共株式会社のイエスカルタが承認を受けました。
キムリアとイエスカルタの特徴
どちらもCAR-T療法に用いられる再生医療等製品であるキムリアとイエスカルタの特徴を紹介します。
| キムリア(2021年2月時点)
|
イエスカルタ(2021年1月時点)
|
|
| 一般名 | チサゲンレクルユーセル | アキシカブタゲン シロルユーセル |
| 構成細胞 |
CAR発現生T細胞 ・患者体重50kg以下※1:0.2×106~5.0×106個/kg ・患者体重50kg超※1: 0.1×108~2.5×108個 ・0.6×108~6.0×108個※2 |
抗CD19 CAR T細胞(生細胞数として):
1.0×106~2.4×106個/kg(最大許容量 2 ×108個) |
| 効能、効果又は性能 | ・再発又は難治性のCD19陽性のB細胞性急性リンパ芽球性白血病
・再発又は難治性のCD19陽性のびまん性大細胞型B細胞リンパ腫 |
以下の再発又は難治性の大細胞型B細胞リンパ腫 ・びまん性大細胞型B細胞リンパ腫 ・原発性縦隔大細胞型B細胞リンパ腫 ・形質転換濾胞性リンパ腫 ・高悪性度B細胞リンパ腫 |
|
投与 |
単回静脈内投与 |
5 分以上かけて30分を超えないように単回静脈内投与 |
|
製造施設(日本向け) |
国内、米国 |
国内 |
|
薬価(患者1人あたり) |
3264万7761円※3 |
3264万7761円※4 |
|
医療機関 |
キムリア治療提供可能施設 |
適切な医療機関 |
|
医療機関から製造施設への輸送方法 |
液体窒素気相下又は -120℃以下で凍結保存した白血球アフェレーシス産物 |
2~8℃に設定された保冷輸送箱で梱包した白血球アフェレーシス産物 |
※1:再発又は難治性のCD19陽性のB細胞性急性リンパ芽球性白血病に用いる場合、※2:再発又は難治性のCD19陽性のびまん性大細胞型B細胞リンパ腫に用いる場合、※3:2021年7月以降、※4:2021年4月21日付
効能、効果又は性能に一部違いがあり、イエスカルタのみに原発性縦隔大細胞型B細胞リンパ腫が認められている一方で,B細胞性急性リンパ芽球性白血病はキムリアのみ使用できます。また、両者の患者1人あたりの薬価は同じ価格で設定されています。
キムリアに加えてイエスカルタが新たに承認されたCAR-T療法用の再生医療等製品ですが、現在も新たな候補製品の臨床試験を実施しているため、今後もCAR-T療法の選択肢が増えていくことが期待できます。
[参考資料]
大嶺 謙 III. キメラ抗原受容体導入T細胞療法 日内会誌 108(7): 1375-1383 (2019)
第一三共株式会社|ヒト体細胞加工製品「イエスカルタ®点滴静注」の国内における 製造販売承認取得のお知らせ – プレスリリース
第一三共株式会社「Medical Library」|イエスカルタ点滴静注(効能・効果、副作用、添付文書等)