がん免疫療法コラム


NK細胞療法
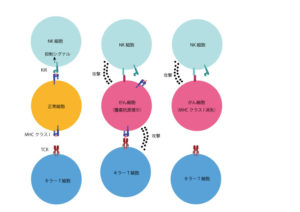
免疫は自然免疫と獲得免疫に分けられます。これまで紹介してきたCAR-T細胞療法やTCR-T細胞療法で使われているT細胞は獲得免疫で中心的な役割を果たしている免疫細胞でした。一方、ナチュラルキラー細胞(NK細胞)は腫瘍細胞やウイルス感染細胞に対する初期の自然免疫反応で重要な役割を果たしている免疫細胞です。
NK細胞表面にはMHCクラスI分子を認識する多様性に富んだKIR受容体が発現しています。KIRは抑制性のシグナルをだす抑制型と活性化シグナルをだす活性型の2種類があり、NKG2A/CやLILRなどの受容体と合わせてNK細胞の活動を制御しています。MHCクラスIを発現している正常自己細胞に対しては、NK細胞は抑制型KIRが働き自己反応を抑制しています。がん細胞の中にはMHCクラスIの発現が低下したり消失しているものがあり、このような細胞に対しては抑制型KIRのシグナルが低下しNK細胞が活性化します。活性化したNK細胞はグランザイムやパーフォリンを放出し、癌細胞のアポトーシスを誘導します。[1]
このようにNK細胞はT細胞とは異なるメカニズムで腫瘍細胞を認識し攻撃するため、T細胞療法を補完する治療法になると期待されています。NK細胞はT細胞に比べて増殖させることが難しいことが大きな課題でした。NK細胞の培養法は活性化や増殖のためのIL-2、IL-15、IL-21などのサイトカインの添加、フィーダー細胞の使用などが検討されてきました。現在ではさまざまな培養条件で高活性のNK細胞を十分な量製造できることが報告されています。しかし、どの製造条件が良いのかの比較は安全性や有効性などさまざまな角度からの検討が必要です。[2]
患者の細胞を使用する自家のNK細胞療法は製造に時間を要し、患者1人ずつのオーダーメイド製造になることからコストも高くなります。NK細胞はT細胞と異なりHLAが完全にマッチングしていないドナーからの細胞を患者に使用してもGvHDなどの問題を起こさないことが知られています。そこで、ドナーからの細胞を使用してあらかじめ大量にNK細胞を製造しておく同種NK細胞療法の開発が進められています。アメリカでは、臍帯血から取ったNK細胞を増殖させた同種NK細胞療法が開発されています。多発性骨髄腫を対象とした臨床試験が実施され、良好な成績を示しています。[3]
また、同種NK細胞にCAR遺伝子を導入する治療法も開発が進んでいます。CAR-NK細胞はCAR-T細胞と同様のCARで認識されるがん細胞に対する高い細胞障害性に加えて、標的抗原の消失などでCARによる認識を逃れたがん細胞に対してもNK細胞のがん認識メカニズムによる細胞障害活性が働くことが期待されてます。MDアンダーソン・がんセンターではCD19 CAR-NK細胞を開発し、再発性/難治性のCD19陽性非ホジキンリンパ腫と慢性リンパ白血病に対する臨床試験を行っています。CAR-T細胞療法でよく起こるサイトカイン放出症候群や神経毒性は見られませんでした。治療を受けた11人中8人の患者(73%)が反応し、7人で完全寛解しましたが、1例は再発しました。投与から12ヶ月以上体内でCAR NK細胞が増殖し維持していることが確認されました。まだ初期段階の研究ですが、今後の進展が期待されます。[4]
また、日本でもiPS細胞からNK細胞を製造する方法が研究されています。iPS細胞から製造したNK細胞は通常のNK細胞と同様の特徴を持ち、マウスで腫瘍増殖抑制効果も確認されています。[5] 無限に増殖できるiPS細胞から品質の揃ったNK細胞を大量に製造できれば、より多くの患者にNK細胞療法を提供できるようになります。
このようにNK細胞療法の研究開発もT細胞に続いて活発になっています。今後の研究開発の進展から目が離せません。
[1] HLAとKIRシステム-基礎と臨床応用. Major Histocmpatibility Complex 2017;24(2): 123-133.
[2] Shaping of Natural Killer Cell Antitumor Activity by Ex Vivo Cultivation. Front Immunol. 2017; 8: 458
[3] Phase I study of cord blood-derived natural killer cells combined with autologous stem cell transplantation in multiple myeloma. British J Maematology, 2017;177(3): 457-466.
[4] Use of CAR-Transduced Natural Killer Cells in CD19-Positive Lymphoid Tumors. N Engl J Med 2020; 382:545-553.
[5] 京都大学iPS細胞研究所プレスリリース「白血病に対する免疫療法を目的とした、無血清条件でのNatural killer細胞誘導」(2019年7月4日)