がん免疫療法コラム


TCR-T細胞療法
日本でも2019年に薬事承認されたCAR-T細胞療法は血液がんで高い有効性を示しています。CAR-T細胞療法はキメラ抗原受容体(Chimeric Antigen Receptor, CAR)を遺伝子改変技術によりT細胞に導入し、体外で増殖させて患者に輸注する治療法です。CARとはがん抗原を認識する一本鎖化した抗体の抗原反応性ドメインとT細胞受容体の刺激を細胞内に伝えるCD3ζ分子の細胞内シグナル伝達ドメイン、CD28や4-IBB等の副刺激受容体分子細胞内シグナル伝達ドメインをつないだ人工的な抗原受容体です。[1]
CAR-Tは血液がんでは大きな成功を収めていますが、固形がんに適用するには課題があります。固形がんの腫瘍抗原の多くは細胞内に存在していますが、CAR-Tは細胞表面の抗原しか認識することができません。
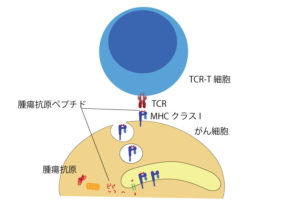
細胞には細胞内の抗原をプロテアソームによりペプチドに分解して、分解されたペプチドをMHCクラスI分子と結合して細胞表面に提示する働きがあります。[2]そこで、MHCクラスIと結合している抗原ペプチドを認識できるT細胞受容体をCAR-Tと同じように遺伝子導入したTCR-T細胞を作成すれば、細胞内に腫瘍抗原がある固形がんも治療できると考えられ、さまざまな研究が行われています。
日本ではタカラバイオがNY-ESO-1特異的TCRを導入したT細胞(TBI-1301)を開発し、滑膜肉腫を対象とした治験を実施しています。[3] TCR-T細胞の製造では患者自身のT細胞に腫瘍特異的なTCRを遺伝子操作で発現させます。T細胞にはもともと発現しているTCR(内在性TCR)があるため、遺伝子導入されたTCRとの競合が起こり、内在性TCRと混合したヘテロ二量体が形成されるなどの問題が生じます。タカラバイオは三重大学と共同でサイレンシング遺伝子(siRNA)技術により内在性TCRの発現を抑制する技術を開発し、この技術を用いてTCR-T細胞を製造しています。[4]
内在性TCRの問題を解決する方法としては他にも、広島大学で、ゲノム編集技術「プラチナTALEN」を利用して内在性TCRをノックアウトする方法が開発されています。[5]
TCRはMHCクラスIと結合しているがん抗原ペプチドを認識するため、患者のHLAタイプに合わせたTCRを使用する必要があります。これをHLA拘束性と呼びます。TBI-1301の治験ではHLA-A*02:01又はA*02:06の患者を対象としています。1
最近、カーディフ大学の研究グループは、個人間で多形化していないMHCクラスIb分子のMR1を標的とすることにより、HLA拘束性がなく誰にでも使用でき、ほとんどの種類の癌を治療できる汎用的なTCR-T細胞療法の可能性を示しました。[6]
このようにCAR-Tの成功に刺激され、遺伝子操作技術の進歩や免疫細胞の研究の進展に支えられて、TCR-T細胞療法の研究開発もホットになっています。
[1] 「CAR-T細胞療法の現状と今後の展望」信州医誌, 2018;66⑹: 425-433.(http://s-igaku.umin.jp/DATA/66_06/66_06_02.pdf)
[2] MBLライフサイエンス「MHCとは?」(https://ruo.mbl.co.jp/bio/product/allergy-Immunology/article/nonself%E2%80%90discrimination.html/)
[3] 医薬品情報データベース臨床試験情報JapicCTI-173514(https://www.clinicaltrials.jp/cti-user/trial/ShowDirect.jsp?clinicalTrialId=28335)
[4] 三重大学リサーチセンター複合的がん免疫療法センター「TCR遺伝子改変T細胞の輸注療法」(http://www.shikuken.jp/research/basic/basic09/)
[5] 広島大学プレスリリース「【研究成果】広島大学発のゲノム編集技術を用いたがんの免疫細胞療法の実用化を目指します~わが国初めてのゲノム細胞創薬技術の開発をAMED事業としてスタート~」(https://www.hiroshima-u.ac.jp/news/58378)
[6] “Genome-wide CRISPR–Cas9 screening reveals ubiquitous T cell cancer targeting via the monomorphic MHC class I-related protein MR1”, NAT Immunol 2020;21, 178-185, (https://www.nature.com/articles/s41590-019-0578-8?proof=true)