がん患者様のためのお役立ちブログ


グリオーマ(神経膠腫)とは? 種類や症状、治療法について解説
グリオーマ(神経膠腫:しんけいこうしゅ)は脳や脊髄に発生する腫瘍で、神経細胞そのものではなく、それを支える「グリア細胞」から生じます(グリア細胞についてはこの後お話しします)。
グリオーマは中枢神経系の腫瘍の中でも比較的多く見られ、良性のものから悪性のものまで、さまざまなタイプが存在します。
今回の記事では、グリオーマの基礎知識から、種類・症状・治療法について詳しく解説します。
【がんの治療の選択肢としておすすめしたい「6種複合免疫療法」】
副作用が少なく、他の治療と併用できる!
6種複合免疫療法は、患者さま自身の免疫細胞を一度体外へ取り出し、活性化・増殖させて体内へ戻すことで、がんと闘う力を高める免疫療法です。
治療法は採血と点滴だけの通院治療です。
6種複合免疫療法をおすすめする理由
- がん3大療法との併用が可能で、ほぼ全てのがんに対応する
- 副作用が少ないため、体への負担も小さい治療法である
- 入院が必要ないため、患者さまの生活のリズムを変えることなく治療を行うことができる
がん治療の選択肢の一つとして、6種複合免疫療法もぜひご検討ください。
今すぐ詳細を知りたい方は、以下よりお問い合わせください。
INDEX
グリオーマ(神経膠腫)とは?
グリオーマ(神経膠腫)は、脳や脊髄にある「グリア細胞」と呼ばれる神経を支える細胞から発生する腫瘍の総称です。
グリア細胞は、神経細胞の働きを助けたり、脳内の環境を整えたりする役割を担っており、この細胞に異常が生じて腫瘍化することでグリオーマが形成されます。
発生する部位や由来となる細胞の種類によって、症状や進行の仕方が異なり、それに応じて治療方針も変わってきます。
グリオーマには、良性のものから悪性度の高いものまでさまざまなタイプがあり、世界保健機関(WHO)の分類により悪性度はグレード1から4に分けられます。
この分類は、腫瘍の進行スピードや再発のリスクを判断するうえでの重要な指標となります。
グリオーマの種類と特徴

グリオーマは、発生するグリア細胞の種類に応じていくつかのタイプに分類されており、それぞれ性質や治療方針が異なります。
これらの分類名は、主に細胞の名前や分類方法に基づいて付けられているため、カタカナや英語由来の専門用語が多く、やや馴染みにくい場合もあります。
ここでは、代表的な4つのタイプについてその特徴をわかりやすく解説します。
星状膠腫(アストロサイトーマ)
星状膠腫は、神経細胞を支える星状膠細胞(アストロサイト)から発生する腫瘍で、良性から悪性までさまざまなタイプが存在します。
進行の程度はWHOのグレード分類によって異なります。
| 発生細胞 | 星状膠細胞 |
| WHOグレード | 1〜4(低悪性度から高悪性度まで幅広い) |
| 主な症状 | けいれん、頭痛、視力障害など |
| 治療法 | 手術を基本に、放射線療法や化学療法を組み合わせる |
| 特徴 | 病理分類により治療法が大きく変わる |
膠芽腫(グリオブラストーマ)
膠芽腫はグリオーマの中でも最も悪性度が高いタイプで、進行の速さと再発率の高さが大きな特徴です。
| 発生細胞 | 星状膠細胞に由来 |
| WHOグレード | 4(最高度の悪性腫瘍) |
| 主な症状 | 頭痛、記憶障害、けいれん、麻痺など |
| 治療法 | 手術+放射線療法+テモゾロミドによる化学療法 |
| 特徴 | 進行が非常に早く、再発率が高い |
乏突起膠腫(オリゴデンドログリオーマ)
乏突起膠腫は比較的まれな腫瘍ですが、治療に対する反応が良好で、長期的なコントロールが期待できるケースもあります。
| 発生細胞 | 乏突起膠細胞 |
| WHOグレード | 2または3(低〜中等度の悪性) |
| 主な症状 | けいれん、頭痛、局所神経症状など |
| 治療法 | 手術+放射線療法・化学療法の併用 |
| 特徴 | 1p/19q共欠失が予後に良好な影響を与える |
上衣腫(エペンディモーマ)
上衣腫は脳室や脊髄に発生する腫瘍で、小児から成人まで幅広い年齢層に見られます。脳脊髄液の流れを妨げることで、頭痛や吐き気などの特徴的な症状が現れることがあります。
| 発生細胞 | 上衣細胞 |
| WHOグレード | 1〜3 |
| 主な症状 | 頭痛、吐き気、水頭症など |
| 治療法 | 手術による摘出が基本。残存腫瘍には放射線療法を併用 |
| 特徴 | 小児では脳室内、成人では脊髄にできやすい |
グリオーマの症状
グリオーマによる症状は、腫瘍の発生部位や大きさ、悪性度によって異なります。
脳や脊髄のどこにできるかによって影響を受ける機能が異なるため、初期症状は多様で、必ずしも明確には現れないことがあります。
代表的な初期症状には以下のようなものがあります。
- 朝方に強く現れる頭痛
- 吐き気や嘔吐
- けいれん発作
- 手足のしびれや運動障害
- 言語障害(言葉が出にくい、話しにくい)
- 視覚の異常(見えづらい、二重に見える など)
腫瘍が進行すると、次第に症状が重くなり、以下のような影響が現れることもあります。
- 記憶障害や集中力の低下
- 意識障害
- 片麻痺などの深刻な運動機能の低下
- 性格や感情の変化(前頭葉が障害される場合)
また、悪性度の高い膠芽腫(グリオブラストーマ)では、こうした症状が短期間で急速に進行し、日常生活に支障をきたすケースも少なくありません。
一方、低悪性度のグリオーマでは進行がゆるやかな場合が多く、症状が軽微なまま長期間続くことで見逃されることもあります。
グリオーマの診断と検査
グリオーマの診断では、症状の確認に加え、画像検査や病理検査を組み合わせて、正確に腫瘍の種類・位置・悪性度を把握することが重要です。
脳内に発生することが多いため、精密な画像検査での評価が診断の第一歩となります。
主な検査内容は以下のとおりです。
| 検査方法 | 内容と目的 |
| MRI(磁気共鳴画像) | 最も基本的な検査で、腫瘍の位置・大きさ・広がりを詳細に確認できる |
| CT(コンピュータ断層撮影) | 緊急時に出血や腫瘍の存在を迅速に把握できる |
| MRS(磁気共鳴スペクトロスコピー) | 腫瘍の代謝物を解析し、良性・悪性の区別を補助する |
| PET(陽電子放出断層撮影) | 腫瘍の活動性や再発の有無を評価する際に用いられる |
| 組織検査(生検) | 確定診断に必要不可欠な検査。
実際に腫瘍の一部を採取し、顕微鏡で細胞の性質を確認する |
画像検査では、腫瘍の境界や脳との位置関係を把握できるため、手術の可否や切除範囲を検討する際にも重要な役割を果たします。
また、最終的な診断には、採取した腫瘍組織を病理学的に評価し、WHO分類に基づいて悪性度(グレード1〜4)を判定します。
近年では、遺伝子検査を含む分子病理学的検査も導入されており、より個別化された治療計画の立案に役立てられています。
グリオーマの治療法と選択肢

グリオーマの治療は、腫瘍の種類や悪性度、患者さまの年齢や全身状態に応じて複数の方法を組み合わせて行われます。
ここでは代表的な治療法である手術、化学療法、放射線療法に加え、近年注目されている分子標的薬や免疫療法についてもご紹介します。
手術
グリオーマ治療において、手術は最も基本となる治療法のひとつです。
腫瘍をできる限り切除することで、症状の改善や腫瘍の進行抑制が期待されます。ただし、腫瘍が脳の重要な機能を担う部位に近い場合には、無理な切除によって後遺症が残るリスクもあるため、安全性とのバランスを考慮しながら慎重に進められます。
近年ではナビゲーションシステムや術中MRIといった先進技術の導入により、より精密で負担の少ない手術が可能になっています。
また、完全切除が難しい場合でも、手術後に放射線療法や化学療法を併用することで、治療効果を高めることが可能です。
化学療法(抗がん剤治療)
化学療法は、手術後に残るがん細胞の抑制や再発予防を目的として行われ、特に悪性度の高いグリオーマにおいて重要な治療法です。主に使用される薬剤は「テモゾロミド(テモダール)」で、放射線療法と併用することで相乗効果が期待されます。経口薬として服用できるため、外来での治療も可能です。
主な副作用には以下のようなものがあります。
- 吐き気・嘔吐
- 倦怠感
- 食欲不振
- 白血球や血小板の減少(感染症や出血傾向のリスク)
副作用には個人差があり、治療中は定期的な血液検査と体調チェックが欠かせません。最近では、分子レベルの特徴に基づいた個別化治療の検討も進められています。
放射線療法
放射線療法は、手術で腫瘍をすべて取り除けなかった場合や、再発のリスクが高いと判断された際に行われる治療法です。高エネルギーの放射線を腫瘍に集中的に照射し、がん細胞の増殖や再発を抑えることを目的としています。治療は通常、1日1回の照射を数週間にわたって繰り返す形で行われ、総照射回数は患者さまの状態や腫瘍の性質に応じて調整されます。
主な副作用には以下のようなものがあります。
- 照射部位の脱毛
- 倦怠感(疲労感)
- 一時的な認知機能の低下
- 食欲不振や吐き気(個人差あり)
こうした副作用は多くの場合一時的であり、症状を軽減するサポートも受けながら治療が進められます。近年では定位放射線治療や強度変調放射線治療(IMRT)など、脳への影響を最小限に抑える高度な技術も活用されています。
分子標的薬
分子標的薬は、がん細胞の特定の遺伝子異常やタンパク質に作用して、がんの増殖や血管新生を抑える治療法です。グリオーマに対しては、「ベバシズマブ(商品名:アバスチン)」が代表的な薬剤で、腫瘍に栄養を届ける新生血管の形成を妨げることで、腫瘍の進行を抑制します。
特に、再発した膠芽腫に対して用いられることが多く、化学療法や放射線療法と併用することで効果が高まるケースもあります。
主な副作用には以下が報告されています。
- 高血圧
- 出血傾向
- 血栓症
- 創傷治癒の遅れ
がんの性質や遺伝子変異の有無によって効果が異なるため、事前の分子診断が治療選択の鍵となります。
免疫療法
免疫療法は、患者さま自身の免疫機能を高めてがん細胞を攻撃させる治療法で、近年さまざまながん種において注目されています。グリオーマに対しては、免疫チェックポイント阻害薬やがんペプチドワクチンなどが研究・臨床試験の対象となっています。
免疫チェックポイント阻害薬は、がん細胞によって抑えられている免疫の働きを回復させる薬で、がん細胞への攻撃力を再活性化させることを目的としています。
一方ペプチドワクチンは、がん特有の抗原を体内の免疫に覚えさせることで、選択的にがん細胞を排除する仕組みです。
これらの治療法は、現時点では標準治療として確立されていないものの、今後の治療選択肢として期待されています。
グリオーマと6種複合免疫療法
グリオーマの治療は、手術・放射線・化学療法の3本柱に加え、近年では分子標的薬や免疫療法といった新しいアプローチも導入され始めています。
しかし、再発や進行を抑えるうえでは、これらの治療法だけでは十分な効果が得られないこともあり、さらなる治療法の開発が求められています。
こうした背景の中で注目されているのが、「6種複合免疫療法」です。
この治療法は、複数の免疫細胞を活性化、増殖させでがんに対してより多角的に働きかけることができます。また、ペプチドワクチンのようにがん特有の抗原を培養している免疫細胞を覚えさせ選択的に攻撃する仕組みがあります。
特に、悪性度の高いグリオーマや再発例において、標準治療後の新たな選択肢となる可能性がある治療法です。
以下、6種複合免疫療法についてさらに詳しく解説します。
副作用が少ない6種複合免疫療法
「6種複合免疫療法」の特徴を3つ紹介します。
①副作用が少なく、体への負担が小さい治療法である
患者さまご自身の免疫細胞を使用するため、抗がん剤のような強い副作用がほとんどありません。
そのため、他のがん治療で治療継続は困難と判断された場合でも、6種複合免疫療法なら治療を継続できる可能性があります。
②がん3大療法との併用が可能で、ほぼ全てのがんに対応する
がん3大療法(外科手術/化学療法/放射線治療)との併用が可能で、一部(T細胞・NK細胞・NKT細胞型白血病/T細胞・NK細胞・NKT細胞型悪性リンパ腫)を除く、ほぼ全てのがんに対応します。
また、手術後に残ったがん細胞にも対応し、がん細胞増殖の抑制、再発・転移の予防にも効果的です。
③入院が必要ないため、患者さまの生活のリズムを変えることなく治療を行うことができる
6種複合免疫療法は、採血と点滴だけの通院治療です。
そのため、入院の必要がなく、患者さまの生活のリズムを変えることなく治療を行うことができます。
6種複合免疫療法の治療効果
以下は、6回(1クール)の治療を終えた患者さまの治療効果を紹介します。
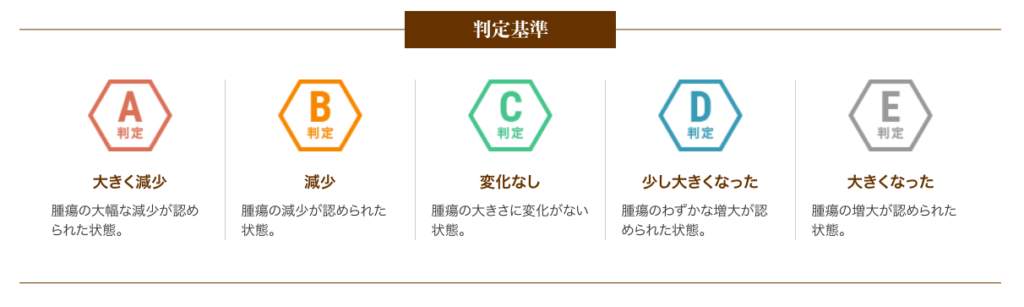

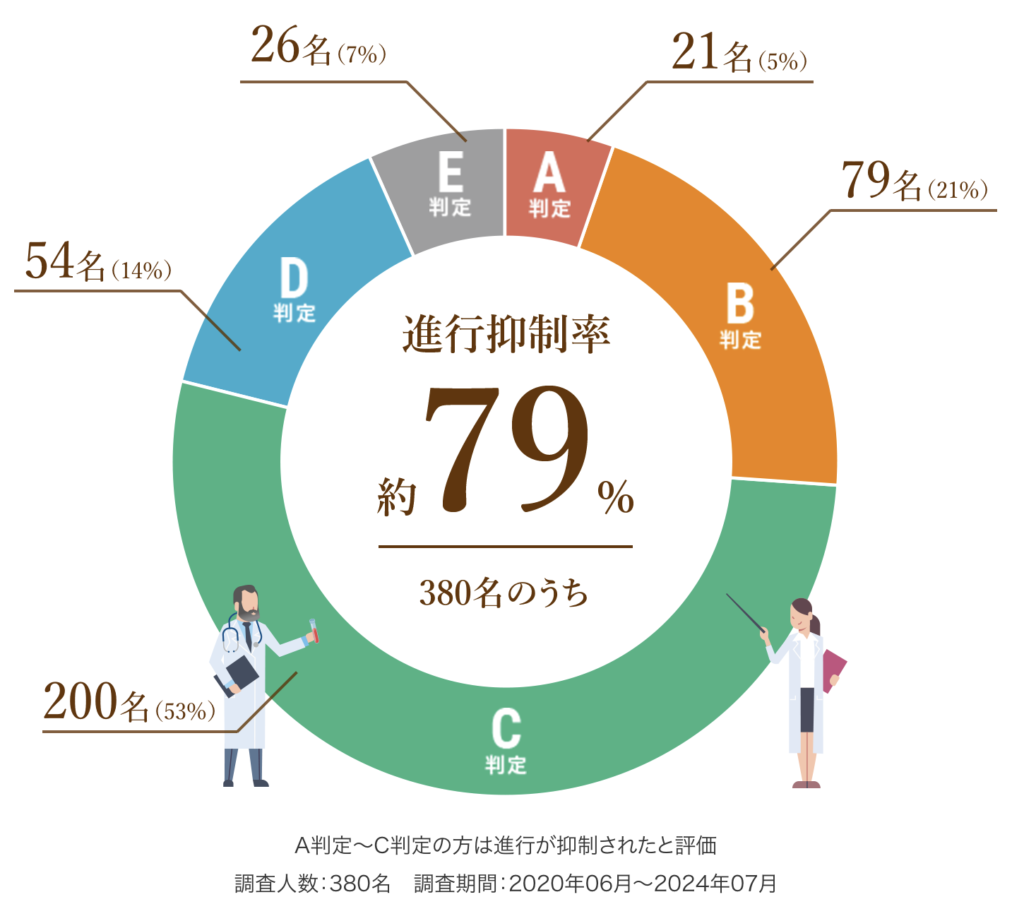
A判定〜C判定の約79%の方は腫瘍の進行が抑制されたと評価し、さらにA判定〜B判定の約26%の方は腫瘍の減少が認められた状態となりました。
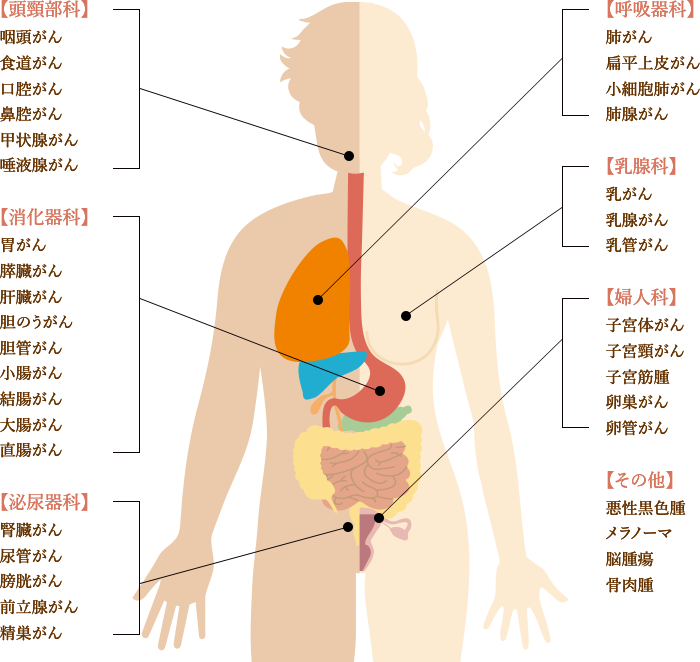
また、6種複合免疫療法の大きな特徴として、さまざまな部位のがんに対応できるという点があります。
以下、6種複合免疫療法で過去に治療したがんの一例です。ほぼ全てのがん種に対応しているため、以下に記載のないがん種や希少がんでも、治療可能です。
詳細は以下よりお問い合わせください。
お電話でのお問い合わせ
専任のスタッフが丁寧に対応いたします。
ご不明な点などございましたら、まずはお気軽にご相談ください。
0120-350-552
受付時間月曜〜金曜/09:00 - 18:00
土曜/09:00 - 13:00